زنگ تفریح 183، طیف سنجی، طیف سنجی 13CN.M.R، طیف سنجی فرابنفش
13C N.M.R:
از دیگر روش های طیف سنجی طیف سنجی رزونانس مغناطیسی هسته ی کربن 13 میباشد. ایزوتوپ کربن 13 در اکثر ترکیبات آلی به مقدار کم وجود دارد. این نوع طیف سنجی کاملا مشابه طیف سنجی 1HN.M.R میباشد. نوع حلال، روش کار دستگاه و ... کاملا مشابه با 1HN.M.R میباشد. البته به دلیل تعداد بسیار کم کربن 13 در ترکیبات آلی قدرت دستگاه در این روش باید خیلی بیشتر باشد.
در هر دو روش طیف سنجی 13CN.M.R و 1HN.M.R از TMS به عنوان مبنا استفاده میشود ولی در روش 13CN.M.R دامنه ی ᵟ بین 0 تا 200 میباشد که در 1HN.M.R بین 0 تا 12 بود. در این روش نیز جداول مرجع وجود دارد که مشخص میکند هر ᵟ مربوط به کدام گروه از ترکیبات آلی میباشد. مهمترین ᵟ های موجود در این طیف سنجی را میتوان در جدولی مثل جدول زیر تقسیم بندی کرد:

رابطه ی چندتایی شدن در این روش نیز به همان شکل 2nI+1 وجود دارد با این تفاوت که در اینجا n تعداد هیدروژن های متصل به خود کربن 13 میباشد.
برخلاف روش 1HN.M.R این طیف سنجی اطلاعاتی درباره ی شیمی فضایی نمونه به ما نمیدهد اما در این روش به علت قدرت زیاد دستگاه اختلافات جزیی کربن ها بر روی نمودار قابل مشاهده است و این امر در شناسایی ساختار ترکیبات حلقوی به ما کمک میکند.
با وجود اینکه این روش از روش 1HN.M.R محدودتر میباشد و کاربرد کمتری دارد ولی در این روش مهارت خواندن نمودارها بسیار مهم میباشد و در مواردی ممکن است ما چندین ساختار برای نمونه رسم کنیم که همگی با نمودارها همخوانی داشته باشند که در این موارد باید در خواندن نمودار دقت بیشتری به عمل آوریم و در صورتی که باز هم نتیجه نگرفتیم باید از طیف سنجی های دیگر استفاده کنیم.
طیف سنجی فرابنفش:
| یکی دیگر از طیف سنجی هایی که به ما در شناخت ساختار ترکیبات کمک میکند طیف سنجی فرابنفش میباشد که اطلاعاتی درباره ی انتقالات الکترونی در نمونه به ما میدهد. ما با دانستن نوع انتقالات الکترونی در یک مولکول میتوانیم درباره ی وجود رزونانس یا وجود پیوندهای π اظهار نظر کنیم. |
 |
ما برای هر مولکول میتوانیم اربیتالی رسم کنیم که اربیتال مولکولی نام دارد. در چنین اربیتالی ما الکترون های شرکت کننده در پیوند ها را در ساختاری رسم میکنیم که به ما نشان میدهد که الکترون در چه نوع پیوندی موجود است. برای یک مولکول اگر اربیتال مولکولی را با تمام ترازهایش بخواهیم رسم کنیم بسیار گسترده خواهد شد لذا فقط اربیتال های π را در نظر میگیریم.
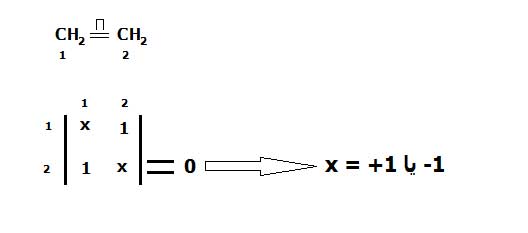
| لذا برای ترکیباتی مثل ترکیبات مقابل همانطور که مشاهده میکنید میتوان دترمینانی رسم کرد که به ما نشان میدهد بین کدام کربن ها پیوند π وجود دارد. اگر دترمینان را برابر با صفر قرار داده و آن را حل کنیم مقدار x را در اختیار ما میگزارد که با توجه به نوع دترمینان تعدادی جواب برای x به دست می آوریم که این جواب ها یا +1 یا -1 میباشد. مقدار و تعداد X هایی که بدست می آوریم تعداد و نوع اربیتال های مولکولی را به ما نشان میدهد. عموما دو نوع اربیتال مولکولی پیوندی و ضد پیوندی در یک ترکیب وجود دارد که از نظز تعداد با هم برابرند و با توجه به اینکه الکترون ها کدام اربیتال ها را پر کنند پیوند π ممکن است تشکیل شود یا نشود. باید توجه داشته باشید که پیوند π از آن لحاظ برای ما اهمیت ویژه ای دارد که عموما انتقالات الکترونی بین پیوندهای π موجود در مولکول انجام میشود. |
 |
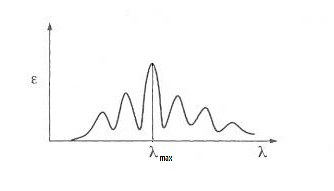
به بالاترین (از لحاظ انرژی) اربیتال پیوندی HOMO و به پایین ترین اربیتال ضد پیوندی LUMO میگویند. با توجه به این مطلب راحت ترین انتقال الکترونی از اربیتال HOMO به LUMO میباشد. هر چه پیوندهای π بیشتر باشد HOMO به LUMO نزدیکتر میشود و انتقال الکترون راحت تر صورت میگیرد. دستگاه طیف سنجی فرابنفش نموداری مثل نمودار مقابل در اختیار ما قرار میدهد که میزان جذب نور فرابنفش توسط نمونه را بر حسب طول موج تابیده شده نشان میدهد. هر چه طول موج نور جذب شده بیشتر باشد نشان میدهد که انتقال الکترونی با انرژی کمتری صورت گرفته.برای مثال اگر دو نمونه داشته باشیم و در یکی طول موج نور جذب شده 400nm و در دیگری 300nm باشد در نمونه ی اول اربیتال HOMO به LUMO نزدیکتر بوده و انتقالات الکترونی راحت تر صورت میگیرد.
| این روش برای رسم ساختار گسترده ی مولکول نمیباشد. بیشترین طول موج نور جذب شده را با λmax نشان میدهند و در این روش عدد λmax مهم میباشد. ما دو نوع λmax داریم که یکی مقدار تئوری میباشد و در جداول برای هر ترکیبی مشخص میباشد و دیگری عملی است که ما توسط دستگاه بدست می آوریم. اگر مقدار λmax عملی به تئوری نزدیک باشد میتوانیم مطمئن باشیم که ساختاری که در طیف سنجی های قبلی برای نمونه رسم کرده ایم درست میباشد و اگر این طور نباشد نشان دهنده ی غلط بودن ساختار حدس زده میباشد. در واقع این روش راهی برای اطمینان از درستی ساختاری میباشد که برای نمونه حدس زده ایم. |
 |
با معرفی طیف سنجی فرابنفش تقریبا میتوانیم بگوییم انواع طیف سنجی های لازم برای رسم ساختار یک ترکیب ناشناخته را به شما معرفی کرده ایم. البته اطلاعاتی که در این بخش ها در اختیار شما قرار داده شده است یک سری اطلاعات کلی میباشد و علاقه مندان برای کسب اطلاعات جامع درباره ی روش های طیف سنجی میتوانند کتاب های پاویا یا سیلورشتاین را مطالعه نمایند. روش های مختلف دیگری نیز برای شناختن ترکیبات مجهول وجود دارد ولی کاملترین آنها روش طیف سنجی میباشد. در آینده حتما درباره ی روش های دیگر نیز اطلاعاتی در اختیار دوستان قرار خواهد گرفت.