آزئوتروپ، نمودار فازی، آزئوتروپ مثبت، آزئوتروپ منفی
نمودارهای فازی:
جوشیدن و معیان دوباره ی یک مخلوط از جمله تغییرات حالت است. این تغییرات به بهترین شکل در نمودارهای فازی نمایش داده می شوند. اگر فشار ثابت نگاه داشته شود، دو پارامتری که می توانند تغییر کنند عبارتند از دما و ترکیب درصد مخلوط. نکته ای که باید در اینجا به آن دقت داشته باشید این است که آزئوتروپ را با امولسیون اشتباه نگیرید.
حداقل جوشش یا آزئوتروپ مثبت:
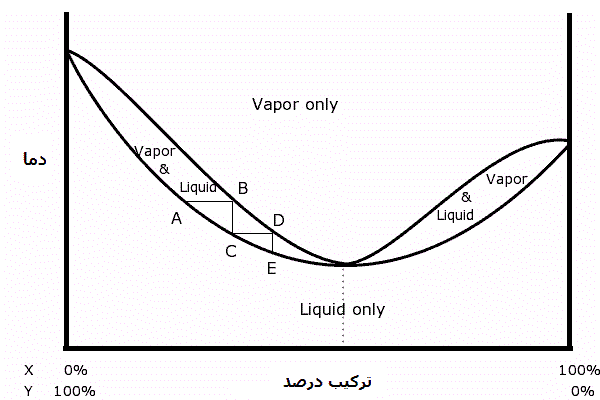 |
نمودار نمایش داده شده در سمت راست یک آزئوتروپ مثبت از ترکیبات فرضی X و Y را نشان میدهد. نمودار پایینی نشان دهنده ی دمای جوش ترکیب درصدهای مختلف میباشد. پایین این نمودار فقط فاز مایع در تعادل میباشد. نمودار بالایی ترکیب درصد بخار در بالای مایع را در دمای مشخص نمایش میدهد. بالای نمودار بالایی تنها فاز بخار در تعادل است. بین این دو نمودار، فاز بخار و مایع در یک زمان در تعادل با هم میباشند. برای مثال گرما دادن به یک مخلوط دارای 25% از X و 75% از Y در دمای AB بخار با ترکیب درصد B را در بالای مایع با ترکیب درصد A ایجاد میکند. آزئوتروپ نقطه ای روی نمودار است که دو منحنی با هم برخورد میکنند. پله های افقی و عمودی مسیر تقطیرهای متوالی را نشان میدهد. نقطه ی A نقطه ی جوش یک مخلوط غیر آزئوتروپ می باشد. بخاری که در این دما جدا میشود دارای ترکیب درصد B می باشد. شکل منحنی ها نشان میدهد که بخار موجود در B نسبت به مایع موجود در A از جزء X بیشتری تشکیل شده است. بخار از نظر فیزیکی از تعادل بخار-مایع جدا شده و در نقطه ی C سرد میشود و تبدیل به مایع میشود. مایع حاصل نسبت به مخلوط در نقطه ی A از جزء X بیشتری تشکیل شده. اگر مایع حاصل دوباره تبخیر شود به نقطه ی D پیشرفت میکند و به همین شکل این روند ادامه میابد تا جایی که ترکیب درصد به درصد آزئوتروپیک میرسد. |
این روند مرحله به مرحله نشان میدهد که چگونه تقطیرهای متوالی نمیتواند یک فرآورده ی تقطیر تولید کند که نسبت به آزئوتروپ از جزء X بیشتری تشکیل شده باشد. اگر مخلوط اولیه ما در سمت راست نقطه ی آزئوتروپ موجود باشد نتیجه ی نهایی مشابه خواهد بود ولی با این فرق که در این حالت تقطیر باعث افزایش جزء Y در مخلوط میشود.
حداکثر جوشش یا آزئوتروپ منفی:
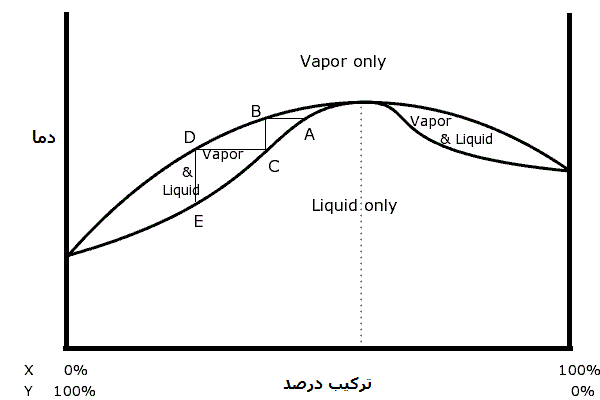 |
نمودار در سمت راست یک آزئوتروپ منفی از ترکیبات سازنده ی X و Y را نشان میدهد. دوباره نمودار پایینی دمای جوش ترکیب درصدهای متفاوت را نشان میدهد و دوباره زیر نمودار پایینی مخلوط در تعادل فاز مایع میباشد. نمودار بالایی مانند قبل دمای معیان ترکیب درصدهای مختلف را نشان میدهد و بالای نمودار بالایی مخلوط در تعادل فاز بخار میباشد. نقطه ی A که در اینجا مشخص شده نقطه ی جوش مخلوطی با ترکیب درصد بسیار نزدیک به درصد آزئوتروپیک میباشد. بخار در همان دما در نقطه ی B بدست می آید. بخار سرد میشود و مایع شده ی آن در دمای نقطه ی C بدست می آید. چون این مثال یک آزئوتروپ منفی است بر خلاف آزئوتروپ مثبت ترکیب درصد فراورده ی تقطیر نسبت به مخلوط اولیه (نقطه ی A) از درصد آزئوتروپیک دور میشود. بنابراین فراورده ی تقطیر نسبت به مخلوط اولیه از جزء X کمتر و جزء Y بیشتر تشکیل شده است. چون این فرایند مقدار بیشتری Y از مخلوط خارج کرده، نسبت به مخلوط اولیه باقیمانده ی تقطیر از جزء X بیشتر و جزء Y کمتر تشکیل شده است. |
اگر نقطه ی A در سمت راست آزئوتروپ انتخاب میشد برخلاف سمت چپ فراورده تقطیر نسبت به مخلوط اولیه از جزء X بیشتر و جزء Y کمتر و باقیمانده ی تقطیر نسبت به مخلوط اولیه از X کمتر و Y بیشتر تشکیل میشد. این امر که هر تعداد تقطیر باعث نمیشود که ترکیب درصد فراورده یا باقیمنده تقطیر از درصد آزئوتروپیک تجاوز کند از جمله خواص آزئوتروپ منفی و در کل از جمله خواص تمام آزئوتروپ ها مییباشد.
چرا دو نمودار وجود دارد؟
نمودارها در نمودار فازی زمانی از هم جدا هستند که ترکیب درصد مخلوط در یک دمای مشخص در فاز مایع نسبت به فاز بخار متفاوت باشد. فرض کنید ترکیب درصد کلی مخلوط 50/50% باشد. میتوان این ساختار را با استفاده از 50% بخار با ترکیب درصد 50/50% و 50% مایع با ترکیب درصد 50/50% تهیه کرد. همچنین میتوان با استفاده از 83.33% بخار 55/45% و 16.67% مایع 25/75% تهیه کرد و همچنین از اختلاط های دیگر به همین شکل میتوان این ترکیب درصد کلی را تهیه کرد. فاصله ی دو نمودار نشان دهنده ی محدوده ی اختلاط درصدی از مایع و بخار است که میتوانند ترکیب درصد کلی را تشکیل دهند.
همچنین نمودار پایینی را میتوان به عنوان مرزی برای ناحیه ای که مایعات در آن در تعادل اند و نمودار بالایی را به عنوان مرزی برای ناحیه ای که بخارها در آن در تعادل اند در نظر گرفت. لزومی ندارد که این دو مرز بر هم منطبق باشند. در واقع ناحیه ی بین این دو مرز یک ناحیه ی بدون صاحب میباشد. تلاش برای انتقال سیستم به نقطه ی میانی پاره خط AB منجر به تشکیل مخلوط مایع A و بخار B میشود ولی در نقطه ی میانی چیزی باقی نمی ماند.