اندازهگیریهای انجام شده روی یک عنصر مصنوعی رادیواکتیو به نام لارنسیم میتواند سوالاتی در مورد موقعیت این عنصر در جدول تناوبی و همچنین ساختار جدول به وجود آورد.

یک تیم بینالمللی از فیزیکدانان و شیمیدانان گزارش دادهاند که انرژی بسیار کمی برای خارج کردن یک الکترون از اتم لارنسیم، عنصر شمارهی ۱۰۳ لازم است. اندازهگیری این انرژی بسیار دشوار است زیرا این عنصر در طبیعت وجود ندارد و تنها در مقادیر بسیار ناچیز قابل سنتز است و به مدت چند ثانیه عمر میکند.
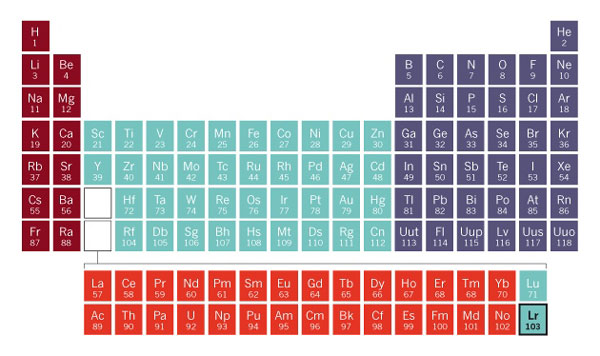
لارنسیم که به نام فیزیکدان Ernest Lawrence مخترع شتابدهندهی ذرات سیکلوترون نامگذاری شده است سنگینترین عنصری است که محققان موفق شدهاند خاصیت بنیادی آن یعنی انرژی اولین یونش (انرژی لازم برای تبدیل اتم به یون با کندن در دسترسترین الکترون آن) را اندازهگیری کنند. این اندازهگیری زیربنای درک دانشمندان از شیمی اتم است اما تاکنون تنها تا اتم einsteinium (عنصر شماره ۹۹) اندازهگیری شده بود.
محققان سازمان انرژی اتمی ژاپن (JAEA) در Tokai عنصر لارنسیم را با شلیک اتمهای بور به هدفی از جنس عنصر Californium که خود ایزوتوپی مصنوعی است ساختند. بدین ترتیب یک اتم لارنسیم-256 (ایزوتوپی دارای 103 پروتون و 153 نوترون) در هر چند ثانیه تولید میشود. نیمه عمر این ایزوتوپ حدود 27 ثانیه است.
محققان این اتمها را در غباری از کادمیم یدید به دام انداختند و آنها را روی سطحی فلزی که تا دمای 2700 کلوین گرم شده بود رسوب دادند. این حرارت شدید سبب خارج شدن یک الکترون از برخی اتمها شد و با شمارش تعداد اتمهایی که از این طریق به یون تبدیل شدهاند، تیم تحقیقاتی موفق شد انرژی مصرف شده توسط آنها را اندازهگیری کند. این مقدار 4.96 الکترون ولت بود که به گفتهی Tetsuya Sato شیمیدان JAEA بسیار کم است. این مقدار در ردهی پنجم پایینترین انرژی اولین یونش در جدول تناوبی است.
آزمایش انجام شده نشان میدهد که خارجیترین الکترون لارنسیم وابستگی بسیار کمی به هسته دارد، مانند اتمهای موجود در ستون سمت چپ جدول تناوبی از جمله سدیم و پتاسیم. این نتیجه مطابق با پیشبینی نظری دانشمندان دانشگاه Tel Aviv است و بسیاری بر سر این موضوع بحث میکنند که این عنصر در کجای جدول تناوبی قرار خواهد گرفت.
جدول تناوبی به شکل ستونها و ردیفهایی چیده شده است که بیانگر آرایش آخرین الکترون (دورترین الکترون) اتمهاست. عناصر اتمها در بخشهای مختلفی به نام بلوکهای s، p، d و f قرار میگیرند. این حروف بیانگر نوع اوربیتال است. (اوربیتالها تودههایی در فضا هستند که احتمال حضور الکترونها در آنها حول هستهی اتم بیشتر است و طبق محاسبات با استفاده از نظریه-ی کوانتوم، s شکل کروی دارد، p دنبلی شکل و اوربیتالهای دیگر بسیار پیچیدهتر هستند.) نحوه و سهولت اتصال یک الکترون به عنصر یا جدا شدن الکترون از آن واکنشپذیری عنصر را تعیین میکند و بر همین اساس عناصر یک ستون از جدول تناوبی رفتار شیمیایی مشابه دارند.
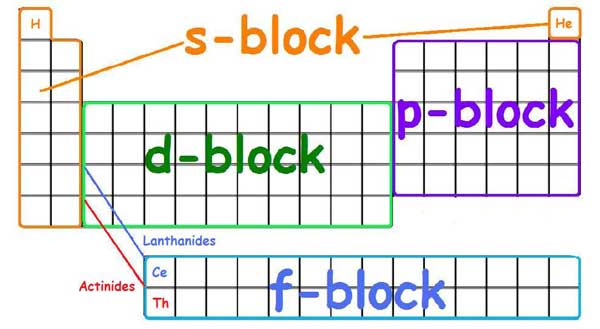
برخی شیمیدانها عقیده دارند که لارنسیم (و عنصر هم خانوادهاش lutetium که یک ردیف بالاتر از آن در جدول تناوبی قرار دارد) خواص شیمیایی مشابه با اسکاندیم و ایتریم در سمت چپ بلوک d جدول تناوبی دارد و باید در پایین این دو عنصر قرار بگیرد. اما در بسیاری از جدولهای تناوبی استاندارد لارنسیم آخرین عنصر دو ردیف سی عنصری به نام لانتانیدها و اکتنیدها است (دلیل نامگذاری این دو ردیف عناصر شروعکنندهی آنها یعنی لانتانیم و اکتینیم است.) و این دو ردیف به عنوان ضمیمه در پایین جدول جای میگیرند. در دیگر جداول تناوبی از جمله جدول تهیه شده توسط اتحادیهی بینالمللی شیمی محض و کاربردی، آیوپاک (IUPAC) تمام بلوک ضمیمهی f به دو جایگاه در پایین اسکاندیم و ایتریم تعلق دارند، در اصل یک زیر مجموعه از بلوک d.
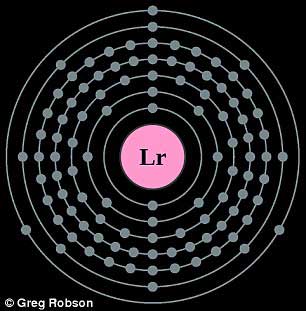 |
آزمایشها و مدلسازیهای عددی نشان میدهد که آخرین الکترون لارنسیم در واقع یک اوربیتال دنبلی شکل p را اشغال می کند. بر اساس تئوریها این اوربیتال نباید اشغال شود اما انرژی آن توسط نسبیت خاص کم میشود زیرا الکترونهای درونی لارنسیم با سرعت بسیار زیاد (کسری از سرعت نور) حول هسته میچرخند و اثر آبشاری بر الکترونهای بیرونی دارند. (تأثیری مشابه در عناصر دیگر از جمله seaborgium فوق سنگین یافت شده است.) برخی از محققان این مطالعه عقیده دارند که بررسیها نشان میدهد این عنصر متعلق به اکتنیدهای بلوک f است؛ به گفتهی Matthias Schadel که سرپرستی گروه JAEA را قبل از بازنشستگی بر عهده داشته است، انرژی یونش بسیار پایین گواه این ادعاست. در دههی ۱۹۸۰ میلادی، Schadel آزمایشهایی انجام داده است که شباهت میان لارنسیم و عنصرهای بلوک f را نشان داده است.
اما William Jensen شیمیدان دانشگاه Cincinnati در اوهایو عقیده دارد که این مطالعات اخیر خلاف این ادعا را اثبات می-کند. از نظر وی بیشتر عناصر اکتنید انرژی اولین یونش بیشتری در مقایسه با عنصرهای بالای خود در جدول تناوبی یعنی لانتانیدها دارند. لارنسیم این روند را به هم میریزد که سبب میشود بیشتر شبیه به عناصر بلوک d باشد. او در مقالهای نظر خود را در مورد قرارگیری لارنسیم در بلوک d جدول تناوبی شرح داده است. Sato معتقد است که با نتایج به دست آمده از این مطالعات نمیتوان پاسخ این تناقضات را داد. به گفتهی Jan Reedjik مدیر بخش شیمی معدنی آیوپاک، این سازمان هنوز نظر قطعی در مورد این مسئله که lutetium و لارنسیم در بلوک f جا دارند یا d نداده است و بررسیهای بیشتر لازم است. به گفتهی Jensen بیشتر شیمیدانها از این جنجال بیاطلاع هستند و این ناراحتکننده است زیرا تمام شیمیدانان باید به داشتن یک جدول تناوبی کاملاً صحیح اهمیت دهند.
منبع:
Nature
ارنست لاؤرنس
exotic molcules
منابع مفید:
اولین انرژی یونش
تاریخچه جدول تناوبی - ۱
تاریخچه جدول تناوبی - ۲
تاریحچه جدول تناوبی - ۳
جدول تناوبی (فلش)
عناصر مصنوعی
شیمی هسته ای
انتهای جدول تناوبی - ۱
انتهای جدول تناوبی - ۲
دردسرهای رادیوایزوتوپ
اوربیتال اتمی - ویکی پدیا