نمایش فاژی عمدتا برای غربالگری پربازده برهمکنشهای پروتئین بهکار میرود...
در سالهای اخیر استفاده از آنتيباديهاي نوترکیبی نظير scFv و VHH ا(Variable Heavy Chain) براي درمان سرطان مورد توجه قرار گرفتهاند. این نوع از آنتیبادیها در مقایسه با آنتیبادیهای منوکلونال بهعلت سايز کوچک و امکان نفوذ بيشتر در بافت به نسبت آنتيباديهاي مونوکلونال، پايداري و حلاليت بالا، نيمه عمر بالا در خون و امکان توليد در سيستمهاي پروکاريوتي دارای ارجحیت هستند. آنتيباديهاي نوترکيب بر عليه مارکرهاي مختلف سرطاني از کتابخانههاي فاژي جدا شدهاند.
بر اساس بررسیهایی که اخیرا صورت پذیرفته، مشخص شده است که قطعات پروتئینی در سطح ویروسهای آلودهکننده باکتریایی قابل نمایشند. این ایده امروزه بهمنظور کلونینگ قطعات ژنومی آنتیبادی به داخل ژنوم پروتئینهای سطحی ویروسها استفاده شده و از آن بهعنوان روشهای Display نام برده میشود. این روشها بعداَ گسترش یافته و امروزه تعدادی از این تکنیکها تحت عنوان Phage Display و Bacterial Display و Ribosomal Display و Mamalian cell line Display شناخته شده هستند. در میان روشهای مذکور، روش نمایش فاژی (Phage Display) از اهمیت بالایی برخوردار است. نمایش فاژی روشی برای بررسی برهمکنش پروتئین با پروتئین، پروتئین با پپتید و پروتئین با DNA است که در آن با استفاده از باکتریوفاژها (Bacteriophage) بین پروتئین و اطلاعات ژنتیکی آن ارتباط برقرار میکنند. سپس این تکنیک برای نمایش دادن پروتئینهایی مثل آنتیبادی گسترش یافت. وجود رابطه بین ژنوتیپ و فنوتیپ در این تکنیک امکان غربالگری (Screening) کتابخانههای بزرگ پروتئینی بهمنظور پیدا کردن و تکثیر یک پروتئین خاص در شرایط آزمایشگاهی را میدهد. شایعترین فاژی که در این تکنیک به کار میرود فاژ M13 و فاژهای رشتهای هستند. اگرچه در این زمینه فاژهای T4، T7 و فاژ λ نیز کاربرد دارند (شکل 1).
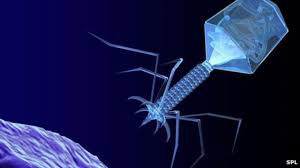
شکل ۱. نمونههایی از ذرات باکتریوفاژ
نمایش فاژی عمدتا برای غربالگری پربازده برهمکنشهای پروتئین بهکار میرود. در مورد نمایش فاژی با فاژ M13، DNA کدکننده پپتید یا پروتئین مورد نظر در ژن پروتئین III و یا VIII، که بهترتیب پروتئین سه و هشت فاژ را کد میکنند، قرار میگیرد (شکل 2). سپس فاژ نوترکیبشده به داخل سلولهای باکتری E.coli مثل TG1، SS320 ER2738, XL1-Blue ترانسفورم میشود.
شکل ۲. نمونههایی از ذرات باکتریوفاژ
اگر از وکتور فاژمیدی استفاده شود ذرات فاژی تا زمانی که باکتری E.coli با فاژ کمکی آلوده نشود از باکتری آزاد نخواهند شد. در این میان فاژ کمکی باعث بستهبندی DNA فاژمیدی با پروتئینهای پوششی میشود. با قرار دادن تعداد زیادی از قطعات DNA در ژنهای III یا VIII میتوان کتابخانهای ایجاد کرد که از آن پروتئینهای مورد نظر قابل جداسازی خواهند بود. با ثابت نمودن DNA یا پروتئینهای هدف روی سطح چاهک، فاژهایی که پروتئین نمایش داده شده روی آن با پروتئین ثابت شده روی سطح چاهک توانایی اتصال داشته باشند باقی مانده، درحالیکه سایر فاژها با شستشو حذف خواهند شد. فاژهای باقیمانده را میتوان استخراج و پس از آلوده نمودن باکتری آنها را تکثیر کرد تا ترکیبی غنی شده از فاژهای مرتبط بهدست آورد. با تکرار این چرخه، که panning نامیده میشود، میتوان نمونه اصلی را باحذف مواد نامطلوب بیش از پیش غنی نمود. فاژهائی که در مرحله آخر panning جدا میشوند برای تکثیر وارد باکتری میشوند و فاژهای تکثیریافته برای غربالگری استفاده میشوند. غربالگری نیز به منظور جداسازی کلونهای اختصاصیتر از میان فازهای غنیشده انجام میگیرد. به منظور غربالگری از پلیتهای الایزا کوت شده با آنتیژن اختصاصی استفاده میشود. شمای شماتیک از اتصال فاژ به باکتری در شکل ۲ نشان داده شده است.
شکل ۳. مراحل اتصال فاژ به باکتری
آلوده شدن فاژ با برهمکنش دومین N2 با پیلی F باکتری شروع میشود، تماس این دو با هم باعث رهاسازی دومن N1 میشود که بعد از آن این دومن به پروتئین TolA موجود در سطح باکتری متصل شده و طبق مراحلی ناشناخته ژنوم فاژ وارد باکتری میشود (شکل ۴).
شکل ۴. نحوه اتصال فاژ به باکتری.
بعد از اینکه ژنوم فاژ وارد باکتری شد، تبدیل به فرم دو رشتهای میشود و پروتئینهای خودش را ترجمه میکند. یکی از این و پروتئینها، پروتئین 5 است که روی تمام ژنوم تکرشتهای فاژ به غیر از بخشی به نام PS یا سیگنال بستهبندی (Packaging Signal) را میپوشاند. این سیگنال در خروج فاژ از باکتری نقش دارد. به طور خلاصه خارج شدن فاژ از باکتری شامل مراحل زیر است:
 مرحله پیشآغازی (Preinitiation): در این مرحله جایگاههای بستهبندی در سطح باکتری تشکیل میشوند. پروتئینهای 1، 11 و 4 در این ساختار نقش دارند (شکل 4).
مرحله پیشآغازی (Preinitiation): در این مرحله جایگاههای بستهبندی در سطح باکتری تشکیل میشوند. پروتئینهای 1، 11 و 4 در این ساختار نقش دارند (شکل 4).  مرحله شروع (Initiation): این مرحله با قرار گرفتن پروتئینهای 7، 9 و ژنوم تکرشتهای فاژ آغاز میشود. در این حالت پروتئینهای 7 و 9 با PS که از یک طرف کمپلکس DNA+PV بیرون زده برهمکنش کرده و باعث آغاز این مرحله میشود.
مرحله شروع (Initiation): این مرحله با قرار گرفتن پروتئینهای 7، 9 و ژنوم تکرشتهای فاژ آغاز میشود. در این حالت پروتئینهای 7 و 9 با PS که از یک طرف کمپلکس DNA+PV بیرون زده برهمکنش کرده و باعث آغاز این مرحله میشود. مرحله طویلسازی (Elongation): از جایگزینی متوالی پروتئینهای 8 با 5 تشکیل شده است.
مرحله طویلسازی (Elongation): از جایگزینی متوالی پروتئینهای 8 با 5 تشکیل شده است. مرحله پیشخاتمه (Pretermination): که در آن کمپلکس پروتئینهای 3 و 6 در انتهای فاژ قرار میگیرند.
مرحله پیشخاتمه (Pretermination): که در آن کمپلکس پروتئینهای 3 و 6 در انتهای فاژ قرار میگیرند.
شکل ۴. ساختار شماتیک جایگاه بستهبندی فاژ در سطح باکتری
 مرحله خاتمه (Termination): که طی آن ساختار فضایی کمپلکس پروتئینهای 3 و 6 تغییر کرده و به رهاسازی فاژ از باکتری کمک میکند.
مرحله خاتمه (Termination): که طی آن ساختار فضایی کمپلکس پروتئینهای 3 و 6 تغییر کرده و به رهاسازی فاژ از باکتری کمک میکند.
حاملهاي فاژميدي تنها داراي منشا همانندسازي باكتريوفاژ خطي و فاقد ژنهاي لازم براي تكثير و بستهبندي ذرات فاژ هستند، بنابراين براي غنيسازي و انتخاب كتابخانه فاژميدي نياز به فاژ كمكي است. فاژكـمكي تكـثير وبستهبندي را انجام داده و سبب رهايي فـاژميد بصورت فـاژ كامل از بـاكتري ميگردد. فاژهای کمکی زیادی موجود است که همه آنها دارای جهشهایی هستند که کارایی آنها را برای بستهبندی و رها شدن از باکتری میکاهد. M13K07 یکی از شایعترین این فاژهای کمکی است که در منشا همانندسازي آن جهشي ايجاد شـده تا توليد و تكثير اين فاژكـمكي با كارايي كمتري انجامپذير ميسازد. همچنين M13KO7 مقاوم به كانامايسين است و اين مقاومت را به باكتري حامل نـاقل هم منتقل ميكند، بنابراين انتخاب باكتري آلـوده به فـاژ كمـكي و نـاقل فـاژميدي آسانتر خواهد بود.
پروتئينها و دومینهاي پروتئيني بسياري بر سطح فاژ نمايش داده شدهاند. در بيشتر اين موارد پروتئين نمايش داده شده بر سطح فاژ توانايي اتصال يا آنزيمي خود را حفظ ميکند. اين نوع نمايش به منظور جداسازي آنتيباديهاي نوترکيب با تمايل بالا و تکامل جهتدار پروتئينها کاربرد دارد. نشان دادن پروتئينها بر روي سطح فاژ يك روش مطمئن براي انتخاب ژنهاي كميابي است كه كدكننده پروتئينها با فعاليت اتصالي هستند. اين تكنيك ميتواند براي نشان دادن مولكولهاي آنتيبادي منوكلونال نيز استفاده گردد. مراحل اين تكنيك در اصل تقليدي از سيستم ايمني هومورال بدن است. در مجموع، بهنظر میرسد که با گسترش این تکنیک بتوان چالشهایی که در رابطه با درمان بسیاری از بیماریها از جمله سرطان تست را کاهش داد.
منابع: