بيش از 50 درصد از جمعیت انساني در سراسر جهان آلوده به اين باكتري هستند

هليكوباكتر پيلوري باسيل گرم منفي، فلاژلداری است كه در شرايط ميكروآئروفيليك زندگي ميكند (شکل 1). اين باكتري در اوايل دهه 80 ميلادي بهوسیله دو محقق به نامهای Marshal و Warren كشف شد. بيش از 50 درصد از جمعیت انساني در سراسر جهان آلوده به اين باكتري هستند. روش انتقال از مدفوع و نیز به طریق خوراکی هست.

بيماريهاي شناختهشده مرتبط با اين باكتري به دو دسته گوارشي و خارج گوارشي طبقهبندی میشود. از بيماريهاي گوارشي ميتوان گاستريت یا التهاب معده، زخم معده و سرطان معده را نام برد. اهميت H.pylori در ايجاد سرطان معده به حدي است كه سازمان بهداشت جهانی آن را كارسينوژن كلاس اول ناميده است. بيماريهاي قلبي عروقي، بيماريهاي ريوي، اختلالات هماتولوژيكي، بيماريهاي پوست، چشم و اختلالات نورولوژيكي از بيماريهاي خارج گوارشي شناختهشده مرتبط با H.pylori است.
كانيسم پاتوژنز:
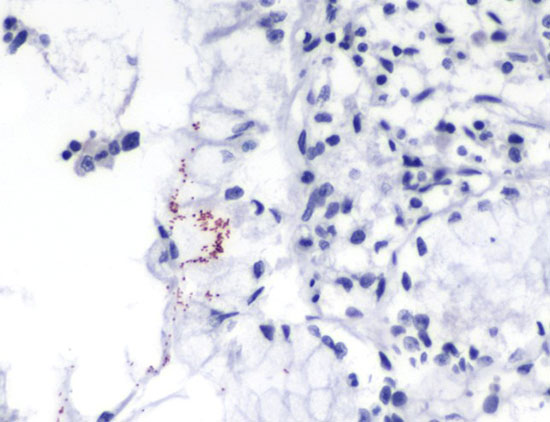
محققین نشان دادند که این اتصال پروتئین Adhesin به اپی تلیال معده برای روند بیماریزایی باکتری ضروری است. محيط معده اسيدي هست، به همين دليل باكتري براي استقرار در موكوس معده با استفاده از آنزيم اورهاز اوره موجود در محيط را تجزيه نموده تا شرايط را براي بقا فراهم كند. این باکتری بهواسطه پروتئین Nap سبب پیشبرد روند بیماریزایی میشود و بهمحض ورود به درون سلول، در سطح لومينال سلولهای اندوتليال، نوتروفيلها و سلولهای تکهستهای را فراخوانده و توليد انبوهي از گونههاي فعال اكسيژن و سيتوكينهاي التهابي را القا میکند (شكل 2). موکوس معده از تک لایه اپیتلیال قطبی ساختهشده که در آن سلولهای اپیتلیال بهطور محکم از طریق ماشینهای اتصال سلولی مثل اتصالات محکم و چسبنده به هم اتصال مییابند. اتصال این باکتری درنهایت سبب التهاب و آسیب رساندن به موکوس معده و ابتلابه بیماریهای گوارشی میشود.
مشابه ديگر پاتوژنهاي شناختهشده، يك سري روشهاي كنترل براي H.pylori پیشنهادشده است. در سطوح تشخيص و درمان قابلکنترل هست که با پیشرفت دانش پروتئین نوترکیب و آنتی بادیهای مونوکلونال جهش بزرگی در رابطه باکنترل و تشخیص این باکتری پدید آمد.

روشهاي تشخيص
۱. روشهای بافتشناسی:
قبل از ارزیابی بافتشناسی، بایستی افراد به مدت 8-6 ساعت ناشتا باشند. بیوپسی موکوسی از معده جداشده و در فرمالدئید 10% تثبیت میشود. سپس نمونهها در پارافین قرار میگیرند. بخشهای 4 میکرومتری از بافت بر روی اسلایدهای شیشهای قرار میگیرد. اسلایدها رنگآمیزی شده و توسط پاتولوژیست بررسی میشود.
۲. تست تنفسی اوره (Urea breath test; UBT):
اساس اين تست بر اندازهگیری دیاکسید کربن موجود در هواي تنفسي است. به بيمار قرص حاوي اوره نشاندار شده با ايزوتوپ كربن 13 داده ميشود. نمونههاي تنفسي در زمان صفر و 20 دقيقه پس از خوردن قرص با استفاده از دستگاه اسپکترومتری جرمی (Mass-spectrometry) اندازهگيري ميشود. علیرغم حساسيت و اختصاصيت بالاي اين تست، به سبب هزينهبر بودن، محققين ژاپني براي استفاده بيماراني كه تحت پوشش بيمه نيستند، تست حساسي با استفاده از آنتیبادی طراحي كردند.
۳. تست سریع علیه آنتیژن Tp؛(Rapid Tp Ag test):
در این تست از مونوکلونال آنتیبادی برضد کاتالاز H.pylori استفاده نمودند. آنزیم کاتالاز از مهمترین آنزیمهای آنتیاکسیدان است که علیه گونههای فعال اکسیژن دارای نقش دفاعی است. نوار تست مورداستفاده پوشيده از مونوكلونال آنتیبادی بر ضد كاتالاز H.pylori است. نمونه مدفوعي رقیقشده بيمار بر روي سطح قرار میگیرد، پس از ده دقيقه انكوباسيون در صورت ظاهر شدن دو خط تست و كنترل، تست مثبت گزارش میشود. حساسيت اين تست 94.7% و اختصاصيت اين روش 95.7% تخمين زده شده است.
۴. تست سریع اوره آز (Rapid urease test; RUT):
اساس تست بر توانايي H.pylori در ترشح آنزيم اورهاز است. تست در زمان گاستروسكوپي انجام میشود. بيوپسي موكوسي گرفتهشده از آنتروم بر روي محيطي حاوي اوره و انديكاتوري مثل فنل رد قرار میگیرد. در صورت حضور H.pylori، اوره به آمونيوم تبدیلشده، به دليل تغيير pH محيط، رنگ معرف از زرد به قرمز تغيير ميكند. پس از 24 ساعت انكوباسيون نتيجه تست قرائت ميشود. محدوديتهاي اين تست به اين شرح است: همه انواع اورهاز بدون توجه به منشأ آن توسط تست تشخيص داده ميشود، به همين دليل ممكن است اورهاز ديگر باكتريهاي موجود در دستگاه گوارش مثل پروتئوس و كلبسيلا تشخيص داده شود. همچنین زمانی که بيمار درمان آنتيبيوتيكي دريافت كرده باشد و شمار باكتريهاي موجود در موكوس کاهشیافته باشد، از حساسيت تست كاسته ميشود.
۵. تست سریع اوره آز به روش ایمنیشناسی (Immunologica rapid urease test; IRUT):
به دليل محدوديتهاي تست اورهاز سريع، IRUT طراحیشده كه در آن از مونوكلونال آنتيبادي برضد اورهاز استفاده ميشود. نمونه موكوسي معده بر روي سطح پوشيده از مونوكلونال آنتيبادي قرار ميگيرد. پس از 15 دقيقه، اين سطح به بخش کنترلکننده pH منتقل ميشود. در اين بخش با استفاده از پمپ، محلولي از سوبسترا حاوي اوره، بخش منتقلشده به مدت 60 ثانيه شستشو داده ميشود. سپس به مدت 55 ثانيه پمپ خاموش ميشود تا واكنش آنزيمي مربوطه انجام شود. در همین زمان پمپ بهصورت معکوس عمل میکند و محلول سوبسترای حاوی اوره، از این بخش خارج میشود، آنگاه پمپ به مدت 5 ثانیه خاموش شده تا تغییرات pH توسط سیستم اندازهگیری شود. حساسيت اين تست 95.2% و اختصاصيت اين روش 98.9% تخمين زدهشده است.
۶. آنتیبادی علیه پروتئین Nap؛ (Anti-Nap Antibody):
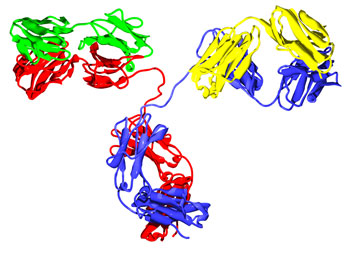
پروتئین Nap یک پروتئین کوچک متشکل از 144 اسیدآمینه بوده که قادر به اتصال به آهن هست. این پروتئین پس از ورود به سلول، نوتروفیل ها و منوسیتها را فعال کرده و تولید گونههای فعال اکسیژن و سیتوکینهای پیش التهابی را القا میکند. درواقع Nap بهعنوان یک لیگاند برای گیرنده موجود در سطح سلولهای ایمنی محسوب میشود.
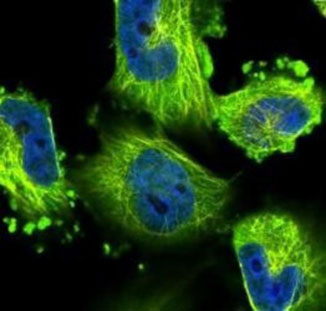
شکل ۶. ارزیابی تشخیصی آنتیبادی ویژه Nap با میکروسکوپ ایمونوفلورسنت
در مطالعهای که صورت گرفت، پپتید متناظر با اسيدآمينههاي 90-70 و 119-97 این پروتئین سنتز شد. از این پپتیدهای سنتتیک برای ایمنیزایی تعدادی موش استفاده شد. مشاهدات حاکی از این بود که تنها موشهای ایمن شده با پپتید متناظر با اسيدآمينههاي 119-97 پاسخ ایمونولوژیکی قوی را نشان دادند. پس از استخراج مونوکلونال آنتیبادی، حساسیت بالای این آنتیبادی تولیدشده، در تشخیص آنتیژن Nap موجود در لیزات سلول کامل H.pylori با آنالیزهای ایمونوبلاتینگ تائید شد. آنالیزهای ایمونوبلاتینگ با استفاده از نشانگرهای اختصاصی علیه یک پروتئین ویژه عمل میکنند و از روشهای سنجش کمی پروتئین محسوب میشوند. همچنین کاربرد تشخیصی این آنتیبادی ویژه Nap با میکروسکوپ ایمونوفلورسنت ارزیابی و تائید شد (شکل 3). از این مونوکلونال آنتیبادی در طراحی الایزای ساندویچی حساس استفاده شد.
۷. آنتیبادی علیه پروتئین Cag؛(Anti-Cag Antibody):
پروتئین Cag، پروتئینی است که ازلحاظ ساختاری با موتیف 5 آمینواسیدی گلوتامات، پرولین، ایزولوسین، تیروزین و آلانین شناخته میشود. با توجه به توالیهای آمینواسیدی اطراف این موتیف، دو نوع Cag شناختهشده است: نوع آسیای شرقی و نوع غربی. در مطالعهای که انجام شد، تعدادی موش با پپتید متناظر با Cag آسیای شرقی ایمن شدند. پس از استخراج مونوکلونال آنتیبادی، اختصاصیت این آنتیبادی از طریق آنالیز ایمونوبلاتینگ وایمونوهیستوشیمی تائید شد. از این آنتیبادی در طراحی الایزایی جهت افتراق Cag آسیای شرقی و غربی استفاده شد. برای این تست دقت 96% حساسیت 88% و اختصاصیت 100% تخمین زدهشده است.
۸. آنتیبادی علیه پروتئین AhpC؛(Anti- AhpC Antibody):
پروتئین AhpC عضوی از خانواده پراکسیردوکسینهاست. پراکسیردوکسینها از فراوانترین پروتئینهای موجود در سلولها میباشند و با اسیدآمینههای سیستئین که در ساختمان خوددارند، در واکنشهای احیایی سلول شرکت میکنند. AhpC به همراه کاتالاز باکتری را در مقابل عوامل دفاعی تولیدشده توسط سلولهای ایمنی حفاظت میکند. به نظر میرسد، چون H.pylori مدتهای طولانی است که در معده انسان زندگی می-کند، بهوسیله مسیرهای ناشناختهای قسمتهایی از ژنهای خود را بهویژه ژنهای کدکننده AhpC را با ژنهای پراکسیردوکسینهای انسانی تبادل میکند و در اثر فرایند نوترکیبی AhpC مشابه پراکسیردوکسینهای انسانی تولید میکند. در مطالعهای که صورت گرفت، پس از استخراج پروتئين 26 کیلودالتونی مربوط به AhpC، از این پروتئین برای ایمنیزایی تعدادی خرگوش استفاده شد. پس از استخراج پلیکلونال آنتیبادی، میزان حساسیت این آنتیبادی با ایمونوبلاتینگ و الایزای غیرمستقیم سنجیده شد. این بررسی نشان داد که استفاده از آنتیبادیهای ویژه آنتیژنهای H.pylori، حساسیت آنزیم ایمونواسی را افزایش میدهد. درواقع این آنتیبادی بهطور اختصاصی به فرم دایمری آنزیم متصل میشود.